편향되지 않은 표현형 기반 스크린으로 전이성 전립선 암에 대한 선택적 치료제 식별
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7962607/
논문제목으로는 치료제를 선별하기 위한 방법에 주안점을 둔것 같고 핵심은 전이성 전립선암에 펜벤다졸과 알벤다졸이 상당한 효과가 있다는 내용입니다.
아래는 원문을 옮긴것입니다.
전립선암 세포가 먼 장기로 전이되면 환자의 예후가 현저히 악화되고 현재 진행된 전립선암을 치료할 수 있는 효과적인 치료 옵션이 없습니다.
fenbendazole, fluspirilene, clofazimine, niclosamide, suloctidil을 포함한 화합물의 하위 집합은 in vitro 및 in vivo 에서 전이성 전립선암 세포에 대해 우선적인 세포 독성과 세포 사멸을 나타냈습니다.
가장 두드러진 약제, 특히 펜벤다졸과 알벤다졸의 생체 이용률은 미셀 또는 나노 입자로 제형화함으로써 개선되었습니다.
향상된 형태의 fenbendazole과 albendazole은 전이가 있는 마우스에서 생존을 상당히 연장시켰고, albendazole 처리된 마우스는 파클리탁셀 처리된 마우스보다 상당히 긴 중앙 생존 시간을 나타냈다.
중요한 것은 이러한 약물이 공격적인 전립선 암 환자의 일반적인 두 가지 임상 조건인 탁산 내성 종양과 골 전이를 효과적으로 표적으로 한다는 것입니다.
요약하면, 전이성 전립선 종양 세포는 특정 약물 종류에 대한 민감도에서 양성 전립선 종양 세포와 다릅니다.
결론적으로, 우리의 결과는 구충제인 albendazole이 전립선 암의 파종 치료에서 표준 요법에 대한 잠재적 보조제 또는 신보조제를 나타낼 수 있음을 강력히 시사합니다.
DTC 파종된 종양세포 : 원래 성장 부위에서 이차부위로 퍼진 종양, 전이된 암을 말하는것으로 보임.
전립선암으로 인한 사망률은 주로 뼈 또는 기타 말단 부위에 파종성 전이가 있는 환자로 제한됩니다.
국소 질환이 있는 남성의 경우 5년 상대 생존율이 100%에 가깝지만, 파종된 암 환자의 비율은 31%에 불과합니다 ( 2 ).
모든 전립선 암 환자의 거의 1/4이 수술이나 방사선 치료 후 전이성 질환을 앓게됩니다 ( 3 – 5).
안드로겐 절제는 종종 재발하는 전립선암의 초기 치료법으로 효과적이지만, 질병은 거의 필연적으로 호르몬 불응성 상태로 진행됩니다.
호르몬 불응성 질환이 있는 남성은 예후가 좋지 않으며 평균 생존 기간은 9 ~ 30개월입니다
또한 상당한 이환율이 이 질환과 관련이 있으며 통증, 골절, 척수 압박, 궁극적으로는 사망을 포함할 수 있습니다.
호르몬 불응성 전이성 전립선암의 관리는 효과적인 치료법의 부족으로 인해 증상 완화로 제한되었습니다.
탁산 기반 화학 요법은 전이성 질환이 있는 일부 남성의 생존율을 향상시켰습니다.
대부분의 환자가 처음에 도세탁셀에 반응하지만, 이러한 암의 대부분은 결국 무감각으로 발전하여 더 공격적이고 화학 요법에 내성이 있는 질병을 유발합니다.
전이성 전립선암 환자의 생존을 연장하기 위해 고안된 대체 치료법을 찾는 것이 시급합니다.
많은 암에서 전이성 병변이 화학 요법과 방사선 요법을 포함한 기존 요법에 제대로 반응하지 않는 것으로 널리 관찰되었습니다.
그 이유는 불분명하지만, 전이 부담의 정도 또는 덜 공격적인 종양에 대해 효과적인 치료에 불응하게 만드는 전이 세포의 내재적 특성 때문일 수 있습니다.
연구에 따르면 이러한 전이성 종양 세포는 특정 세포 표면 마커의 발현을 포함하여 줄기 세포와 유사한 특성을 얻을 수 있습니다.
따라서 화학 요법제 및 전리방사선에 대한 내성이 증가했습니다.
마찬가지로, 전이성 캐스케이드 동안 이러한 세포는 특정 물질에 대한 감수성을 획득할 수도 있습니다.
이러한 취약성이 전이성 전립선 암 치료를 위한 효과적인 약제를 개발하는데 표적이 될 수 있다고 가정했습니다.
이 가설을 테스트하기 위해 1120 개의 약물 라이브러리를 사용하여 고도로 전이성 및 전이성이 낮은 전립선 암 세포의 여러 패널의 상대적 차등 세포 독성을 테스트했으며, 대부분은 FDA (Food and Drug Administration) 승인을 받았습니다.
흥미롭게도, 몇몇 약물은 시험관 내 및 생체 내 모두에서 높은 전이 잠재력을 가진 종양 세포에 대해 증가된 세포 독성을 보여주었습니다
이러한 약물은 이미 다른 목적으로 인간에게 사용되고 있기 때문에 새로 발견된 약물은 기존 약물 투여 요법을 사용하여 인간 임상 효능 연구에 빠르게 진입하거나 알려진 약동학 및 약력학적 프로파일을 기반으로 개선될 수 있습니다.
우리의 연구는 전이성 종양을 효과적으로 치료할 수 있는 약물에 대한 스크리닝을 수행하는 것이 가능함을 보여주고 이러한 새로 확인된 약물이 약물 개발에서 "재목적 약물" 접근법의 예가 될 수 있음을 시사합니다.
여기까지가 요약과 함께 간단한 소개의 글입니다.
실험에 관련된 내용은 생략하고 나노입자를 만드는 부분은 간략하게나마 정리해봅니다.
100 % DMSO 또는 DMSO, NMP, tween-80 및 cremophor EL (DNTC)의 혼합물에서 1 : 3 : 2 : 2 비율로 제조되었습니다.
생성된 혼합물은 안정했고 실온에 보관했다.
나노 입자는 에멀젼-용매 증발 기술을 사용하여 제형화되었고 PLGA-PEG 접합체는 설명된대로 합성되었습니다 ( 20).
PLGA (MW4.2 kD, 40 mg) 및 PLGA-PEG (10 mg)를 아세톤에 용해시키고 알벤다졸 (5 mg)과 혼합했습니다.
용액은 일정한 균질화와 함께 느린 주입에 의해 PVA의 2 % 수용액 (80 % 가수 분해, MW9-10kD)으로 유화되었다.
NP 크기 분획은 3,000 xg에서 5 분 동안 및 90,000 xg에서 2 시간 동안 초 원심 분리하여 회수되었습니다.
나노 입자의 크기 분포는 He-Ne 레이저가 장착된 Malvern Zetasizer 동적 광산란 시스템을 사용하여 조사되었습니다.
나노 입자의 알벤다졸 로딩은 298 nm에서 UV-VIS 분광법에 의해 결정되었습니다.
일반인이 만들기는 어렵겠죠^^ 하지만 이런 방식으로 나노화했다는 정도로 알고 있으면 될것 같습니다.
결론적으로 전이성 전립선암에 알벤다졸을 사용해야 한다고 주장하는 몇가지 이유
=펜벤다졸이 효과가 있지만 수의용 약이라서 임상 적용의 애로를 말하는 것 같다.
=펜벤다졸이 중요한 이유중 하나가 파클리탁셀 내성 전립선암에 대한 세포 독성을 가졌기 때문.
=Albendazole 치료는 전이성 전립선 암에 대한 현재의 최전선 치료인 paclitaxel보다 우수하지는 않지만 비슷했다.
=또한 albendazole이 폐나 뼈에 있는 전립선암 세포의 성장을 억제한다는 것을 증명했다.
=펜벤다졸과 알벤다졸만이 부모 세포에 비해 PC-3 및 DU-145 내성 세포 모두에서 더 큰 항 종양 활성 (낮은 ED50으로 표시됨)을 나타냈습니다.
=다만 흡수가 잘 안되기에 나노 제형화가 필요하다.
=FDA에서 승인한 생분해성 및 생체 적합성 PLGA-PEG 나노 입자 제형이 인간의 임상 적용에 더 유용하고 효과적이다.
=albendazole이 즉석 DNTC 또는 나노 입자 기반 제형에 용해되었을때 폐와 뼈의 종양 부담을 줄여 심각한 항 종양 활성을 나타내어 결과적으로 이러한 마우스의 생존율이 향상되었다.
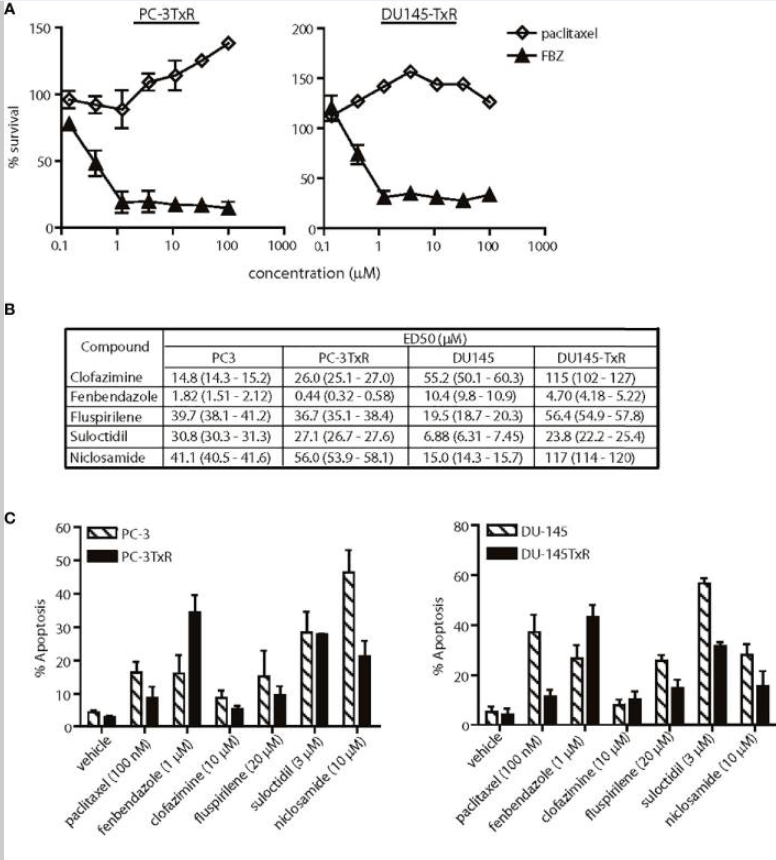
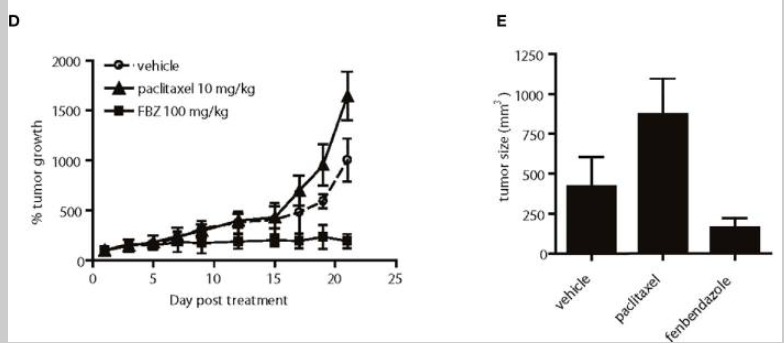
파클리탁셀 내성 전립선 암 세포에서 lead agents의 효과.
(A) 파클리탁셀 내성 전립선 암 세포에서 파클리탁셀 및 펜벤다졸 (FBZ)의 세포 독성 효과.
FBZ-DNTC는 1μM 이상의 용량에서 두 세포주에서 파클리탁셀 단독보다 유의하게 더 많은 세포 독성을 나타냈습니다.
(B) 파클리탁셀 민감성 및 내성 세포주에서 약물의 ED50 비교.
(C) 파클리탁셀 민감성 및 내성 세포주에서 각 약물들에 의해 유도된 세포 자멸사 백분율.
(B, C)의 데이터를 비교하면 , FBZ는 두 파클리탁셀 내성 전립선 암 세포주에서 유의하게 세포 독성 / 아폽토시스가 더 많은 유일한 약물이었다.
(D) DNTC에서 DNTC 단독, 파클리탁셀 또는 FBZ로 처리한 후 피하 PC-3TxR 종양의 상대적 성장.
치료는 3주 동안 주당 3회 제공되었다.
FBZ는 파클리탁셀 또는 비히클과 비교하여 종양 성장을 유의하게 억제했다.
(E) 연구 종료시 각 치료 그룹의 종양 크기 평균.
표시된 데이터는 평균 ± 95 % 신뢰 구간, 그룹당 N = 10, p <0.01입니다.
파클리탁셀과 벤즈이미다졸의 차이
=미세관 중합을 표적으로 하여 유사하게 작동.
=벤즈이미다졸의 튜불린 결합 부위는 파클리탁셀 또는 빈블라스틴에 의해 표적화된 부위와 뚜렷하게 다르다.
=벤즈이미다졸은 미세소관 외부에 위치한 부위에 결합하는 반면 다른 부위는 미세관 내강의 이량체 내 경계 근처에 결합합니다.
=알벤다졸과 펜벤다졸의 활성 대사산물은 대부분의 화학요법 약물과 달리 인간 유방암 저항성 단백질 (Bcrp1 /ABCG2), 다약제 저항성 단백질 (MRP) 2 또는 P-당 단백질 (Pgp)의 기질이 아니다.
가장 중요한 것은 약물의 항 종양 범위와 안전성, 장기치료. 그리고 벤즈이미다졸의 항 종양 효과
=시험관 내 실험의 경우 낮은 마이크로 몰 범위였고 생체 내에서 100mg /kg이었다 .
=인간이 달성할 수 있는 약리학적 수준. ( 56 ).
=비교적 양성인 안전성 프로필
=다른 약물에 내성이 있는 환자에서도 전이성 암의 장기 치료에 사용할수 있어야 한다.
=진행성 간세포 암종 환자를 대상으로 한 알벤다졸의 소규모 임상 시험에서 유망한 항 종양 활성 (질병의 안정화)과 잘 견디는 부작용이 나타났다 ( 58 ).
=경구 전달을 위한 잠재적으로 관련된 화합물 mebendazole의 수용성 유도체가 최근에 상당한 항암 활성 (가질 것으로 나타났다 (59) ).
=전립선 암에서 이러한 항 종양 효과는 알벤다졸, 옥시벤다졸 및 메벤다졸을 포함한 벤즈이미다졸 화합물 계열의 다른 구성원에서도 관찰되었다 ( 36 –38 ).
56번 논문은 신경낭포증 치료에 쓰인 알벤다졸의 경우를 말하는데, 그만큼 일상적인 용량으로 가능했다는 표현임 .
58번 논문에서 알벤다졸은 28일 동안 10mg /kg /일로 2회 분할된 용량으로 경구 투여되었다.
이 논문에서는 알벤다졸과 같은 특정 약물이 전파된 진행성 전립선 암 치료에 강력한 항암제일 수 있음을 보여준다.
특히 펜벤다졸은 여러 약제들 중 더 큰 생존 촉진 효과를 보여 주었다.
펜벤다졸은 또한 골치덩어리였던 파클리탁셀 내성 전립선 암에 대한 세포 독성이었다.
요약하면, 전이성 및 탁산 내성 전립선암 세포에 대해 강력한 항 종양 활성이 있듯이 다른 전이성 암에서도 이와 같은 항전이성 약물 검사를 통해서 말기암 환자의 수명을 연장할 수 있는 약물 등급을 나타낼 수 있어야겠다는 표현.
즉 FDA가 인정한 약들중에서 효과 있는 약들을 연구자들 방법으로 검증해서 말기암 환자의 수명연장을 가능하게 ...
이 논문에서 다룬 항암 효과가 있는 몇몇 약물들
Niclosamide는 촌충에서 산화적 인산화 과정을 분리하는 것으로 나타났으며 암세포에서 다중 생존 신호 전달 경로를 억제할 수 있습니다 ( 39 , 40 ).
강력한 항 정신병 약물인 Fluspirilene은 Ca 2+ 채널을 차단하여 작용합니다 ( 41 ).
항 종양 활성은 충분히 연구되지 않았지만, 명백한 세포 손상없이 종양 세포에서 자가 포식을 촉진하는 것으로 나타났습니다 . ( 42 )
나병 및 결핵 치료제인 클로파지민 (Clofazimine)도 결장암 및 췌장암 치료를 위해 연구되었습니다. ( 43 , 44).
연구에 따르면 클로파지민은 인지질 A2의 활성을 유도하여 세포 증식을 억제합니다 ( 26 , 45 ).
Suloctidil은 cyclo-oxygenase 활성을 억제하여 세포 증식에 영향을 미칠 수 있지만 혈관 확장제로 보고된 작용 기전은 혈소판 응집 억제와 관련이 있습니다 ( 27 ).
'암 종류별 총정리 > 전립선암' 카테고리의 다른 글
| 전립선암 치료제 자이티가 약물정보 (0) | 2021.12.03 |
|---|---|
| 전립선암 (0) | 2021.06.17 |
| 암세포가 잠에 드는 이유 Why cancer cells go to sleep (0) | 2021.06.17 |
| 유방암, 전립선암 식약처 (0) | 2021.05.11 |
| 전립선암(Prostate cancer, Pca) 치료를 위한 대체약 (0) | 2021.01.03 |